LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
Kamis, 17 November 2016
alkalinitas,
BOD,
CO2,
danau tambak boyo,
densitas,
diversitas,
DO,
ekosistem,
ekosistem danau,
kecerahan,
Kuliah & Sekolah,
Laporan,
lentik,
parameter,
pH,
plankton,
suhu,
TSS,
vegetasi
Edit
LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN - Hallo semuanya Pembaca Berita, Pada postingan berita kali ini yang berjudul LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN, telah di posting di blog ini dengan lengkap dari awal lagi sampai akhir. mudah-mudahan berita ini dapat membantu anda semuanya. Baiklah, ini dia berita terbaru nya.
Judul Posting : LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
Link : LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
Anda sedang membaca posting tentang LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN dan berita ini url permalinknya adalah https://nyimakpelajaran.blogspot.com/2016/11/laporan-ekosistem-danau-ekologi-perairan.html Semoga info lowongan ini bisa bermanfaat.
Judul Posting : LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
Link : LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
EKOSISTEM DANAU
EKOLOGI PERAIRAN
Amara Faiz Wriahusna
14/367219/PN/13822
Teknologi Hasil Perikanan
Intisari
Ekosistem merupakan sistem yang terdiri atas seluruh organisme dan lingkungan abiotik yang terjadi aliran energi dan materi. Ekosistem danau merupakan perairan menggenang (lentik). Tujuan dari praktikum ini adalah untuk mempelajari karakteristik ekosistem lentik (perairan menggenang) dan faktor-faktor pembatasnya, mempelajari cara-cara pengambilan data tolokukur (parameter) fisik, kimia, biologik suatu perairan lentik, mempelajari korelasi antara beberapa tolokukur lingkungan dengan populasi biota perairan (plankton dan bentos), serta mempelajari kualitas perairan lentik berdasarkan atas indeks diversitas biota perairan. Praktikum ini dilaksanakan pada Kamis, 17 Maret 2015 pada pukul 14.00-16.30 WIB dan berlokasi di danau Tambak Boyo Yogyakarta. Dari danau tersebut dibagi menjadi empat stasiun dan pada setiap stasiun dilakukan pengukuran tiga parameter yaitu biologi (Vegetasi, diversitas plankton, dan densitas plankton), kimia (pH, DO, CO2 bebas, alkalinitas, BOD0, BOD5), fisika (TSS, suhu, kecerahan, warna air). Dari hasil yang didapat, berdasarkan diversitas plankton stasiun yang paling baik adalah stasiun dua.
Kata kunci : alkalinitas, BOD, CO2, DO, danau Tambak Boyo, densitas, diversitas, ekosistem, kecerahan, lentik, parameter, pH, plankton, suhu, TSS, vegetasi
PENDAHULUAN
Danau adalah suatu bentuk ekosistem yang relatif kecil dan menempati suatu daerah pada permukaan bumi dibanding habitat laut dan daratan. Danau merupakan perairan menggenang yang memberikan berbagai fungsi yang menguntungkan bagi kehidupan manusia. Selain itu, danau juga berfungsi sebagai habitat biota perairan. Saat ini, danau mulai berubah fungsinya akibat aktifitas manusia di bidang industri yang dapat menurunkan dan mencemari kualitas perairan. Perubahan ekositem dapat mempengaruhi keseimbangan perairan, dan perubahan tersebut dapat terjadi secara alami atau karena aktivitas manusia tersebut.
Peraiaran sendiri dibedakan menjadi dua, yaitu perairan mengalir (lotik) dan perairan menggenang (lentik). Danau merupakan contoh perairan menggenang (lentik) dan zonasenya dibagi menjadi dua, yaitu zonase bentos dan kolam air (Cole, 1988). Danau merupakan suatu badan air yang menggenangi suatu cekungan dipermukaan bumi dengan luas mulai dari beberapa meter persegi hingga ratusan meter persegi dengan jumlah air yang relatif banyak (Rumihat, 2007). Ciri arus air danau sangat lambat atau tidak ada arus sama sekali, oleh karena itu waktu tinggal air dapat berlangsung lama dan arus tersebut dapat bergerak ke segala arah (Effendi, 2003). Berdasarkan proses terjadinya danau dikenal dengan danau tektonik yang terjadi akibat gempa dan danau vulkanik yang terjadi akibat aktivitas gunung berapi (Barus, 2004). Berdasarkan materi organiknya yang di produksi dikelompokkan yaitu danau oligotropik, eutropik, dan distropik (Paney, 1986). Ekosistem danau memiliki empat zona (daerah) yakni litoral, limnetik, profundal dan bentik (Soegianto, 1994).
Organisme makrobentos hingga yang berukuran mikroskopis adalah suatu organisme yang merupakan penghuni dalam ekosistem danau (Wibisono, 2005). Kualitas air mengacu pada kandungan polutan dalam air terhadap ekosistem didalamnya. Mikroorganisme dalam perairan semisal plankton mempengaruhi kesuburan. Sedang kesuburan itu sendiri dibagi menjadi tiga tingkat yakni rendah, sedang, dan tinggi yang akan mempengaruhi pertumbuhan biota perairan (Khairuman, 2003).
Tujuan dari praktikum ini adalah untuk mempelajari karakteristik ekosistem lentik (perairan menggenang) dan faktor-faktor pembatasnya, mempelajari cara-cara pengambilan data tolokukur (parameter) fisik, kimia, biologik suatu perairan lentik, mempelajari korelasi antara beberapa tolokukur lingkungan dengan populasi biota perairan (plankton dan bentos), serta mempelajari kualitas perairan lentik berdasarkan atas indeks diversitas biota perairan.
METODE
Praktikum ini dilaksanakan pada Kamis, 17 Maret 2015 pada pukul 14.00-16.30 WIB dan berlokasi di danau Tambak Boyo Yogyakarta.
Alat-alat yang digunakan dalam praktikum ini adalah water sampler , meteran atau penggaris, thermometer, botol oksigen, Erlenmeyer, gelas ukur, pipet ukur atau buret, pipet tetes, mikroburet, aerator, ember plastic, jarring plankton , kertas label dan pensil.
Bahan-bahan yang digunakan yaitu kertas pH, kertas saring, atau milipore, dengan pori 0,45µm , timbangan analitik, larutan MnSO4, larutan reagen oksigen, larutan H2SO4 pekat, larutan 1/80 N Na2S2O3, larutan 1/44 N NaOH, larutan 1/50 N H2SO2, dan larutan indicator amilum, larutan Indikator PP, larutan indicator Methyl Orange (MO), larutan 4 N H2SO4, larutan 0,1 Kalium Permanganat, larutan 0,1 N Amonium oksalat dan larutan 4% formalin.
Pada masing-masing stasiun pengamatan parameter fisika (suhu air, suhu udara, TSS, warna air dan kecerahan), parameter kimia ( kandungan O2 telarut, CO2 bebas , alkalinitas, Ph, BO, BOD0, BOD5), dan parameter biologi (densitas dan diversitas plankton). Pengamatan ekosistem danau dibagi menjadi empat stasiun pengamatan.
Pada pengamatan parameter fisika yang diamati adalah warna air, kecerahan air yang diukur dengan menggunakn secchi disc, suhu air dan suhu udara diukur dengan termometer, dan TSS dengan menggunakan metode gravimetri. Untuk menghitung TSS mengunakan rumus: Kandungan TSS =(1000/y) x (B-A) mg/l, Y merupakan volume air sampel, A adalah massa kertas saring sebelum penyaringan, B adalah massa kertas penyaring setelah penyaringan.
Pada parameter kimia yang diukur adalah DO dengan menggunakan metode Winkler dengan rumus:DO = (1000/50) x Y x 0,1 mg/l, Y merupakan volume larutan 1/80N Na2S2O3 untuk titrasi. Untuk CO2 bebas digunakan metode alkalimetri dengan rumus: Kandungan CO2 bebas=(1000/50) x C x 1 mg/l , C merupakan volume titrasi 1/44N NaOH yang digunakan untuk titrasi. Alkalinitas digunakan metode alkalimetri untuk mengukurnya dengan rumus Kadar CO32- = (1000/50) x C x mg/l = x; Kadar HCO3- = (1000/50) x D x mg/l= y; Alkalinitas total = x + y mg/l, dimana C adalah volume larutan 1/50N H2SO4 dan D adalah volume H2SO4 untuk titrasi. BOD5 diukur dengan mengambil air sampel ke botol oksigen dan diinkubasi selama 5 hari. Kemudian ditambahkan 1ml 4 N H2SO4, 2 tetes 0,1 N Kalium Permanganat, dan 2 tetes ammonium hidroksida, selanjutnya analisis sama seperti DO. Rumus pengukuran Kandungan BOD5 = (1000/vol air sampel) x (B-A) X 0,1 mg/l . A merupakan hasil analisis DO segera dan B adalah hasil analisis kandungan DO setelah 5 hari. BO diukur sampel air 50 ml ditambahkan 3 tetes larutan 0,1 N kalium permanganat kemudian dipanaskan, 10 ml 0,01 N asam oksalat dan didinginkan hingga 60oC, tambahkan larutan 0,01 N Kalium Permanganat. Perhitungan BO dengan menggunakan rumus: Kandungan BO=(1000/50) x (((10+a) x f)-10) x 0,3163 mg/l , dengan a adalah volume titrasi larutan 0,01 N kalium permanganat dan f adalah faktor korelasi kalium permanganat.
Parameter biologi yang diukur adalah diversitas plankton dihitung dengan rumus Shannon-Weiner yaitu H= -∑(ni/N) 2 log ni/N, H merupakan indeks keanekaragaman, ni adalah cacah individu suatu genus, dan N adalah cacah individu seluruh genera dan densitas plankton menggunakan rumus Ď=(S-1)/Y, Ď merupakan densitas plankton, S merupakan jumlah titik cuplikan yang diambil, Y adalah luas area kajian.
HASIL DAN PEMBAHASAN
Berikut adalah hasil dari praktikum yang telah dilakukan
TABEL PENGAMATAN EKOSISTEM DANAU
Praktikum ini dilaksanakan di danau Tambak Boyo Yogyakarta, dan pengamatan dibagi menjadi empat stasiun. Praktikum ini dilaksanakan pada pukul 14.00-16.30 WIB dan kondisi saat praktikum cerah. Pada stasiun satu, merupakan pintu masuk air dari sungai ke danau. Kondisi perairan pada stasiun satu tercemar sampah plastik dan sampah organik seperti daun-daun dan ranting pohon.
Dari grafik suhu udara vs stasiun, suhu udara teringgi berada pada stasiun dua yaitu 32oC sedangkan suhu udara terendah berada pada stasiun satu yaitu 27,5oC. Menurut Pratiwi et al. (2004), semakin tinggi suatu tempat maka suhu udaranya semakin rendah. Ketinggian dari semua stasiun adalah sama namun terdapat perbedaan suhu, hal ini dikarenakan adanya vegetasi yang tumbuh di sekitar stasiun. Semakin rimbun vegetasi maka semakin rendah suhu udaranya.
Menurut Effendi (2003), air dapat menyerap panas dengan mudah dan menahan panas lebih lama, sehingga kapasitas panas dalam air cenderung tetap. Suhu air yang lebih tinggi dari suhu udara, disebabkan karena air memiliki kerapatan molekul yang lebih tinggi sehingga mampu menyimpan panas lebih lama dibandingkan molekul udara. Dari grafik suhu air vs stasiun, dapat diketahui bahwa hanya stasiun satu yang cocok dengan teorinya karena suhu air lebih tinggi dibanding suhu udara sedangkan stasiun lain tidak. Hal ini mungkin terjadi karena saat pengukuran suhu, cuaca sangat panas dan udaranya kering sehingga dapat menyebabkan suhu udara lebih tinggi.
Dari grafik kecerahan vs stasiun, dapat diketahui kecerahan paling tinggi berada pada stasiun empat sedangkan kecerahan paling rendah berada pada stasiun satu. Hal ini terjadi karena pada stasiun satu yang merupakan pintu masuk air dari sungai terdapat saringan yang menyebabkan banyak sampah yang menumpuk disana sehingga kecerahan dari air pun juga ikut berkurang. Nilai kecerahan sangat dipengaruhi oleh adanya cuaca, kekeruhan padatan yang tersuspensi dan terlarut (lumpur dan pasir halus) (Effendi, 2003).
Dari grafik TSS vs stasiun, dapat diketahui bahwa jumlah TSS tertinggi berada pada stasiun empat sedangkan jumlah TSS terendah berada pada stasiun satu. Menurut Tarigan (2003), Zat padat tersuspensi merupakan tempat berlangsungnya reaksi-reaksi kimia yang heterogen, dan berfungsi sebagai bahan pembentuk endapan yang paling awal dan dapat menghalangi kemampuan produksi zat organik di suatu perairan. Dengan demikian, grafik TSS berbanding terbalik dengan grafik TSS ini.
Dari densitas plankton vs stasiun, dapat diketahui bahwa densitas plankton tertinggi berada pada stasiun empat sedangkan densitas plankton terendah berada pada stasiun tiga. Kehadiran karbon dioksida (CO2) sangat erat kaitanya dengan kuantitas atau jumlah keberadaan kadar oksigen dalam air, dimana kenaikan kadar karbondioksida akan selalu diikuti oleh penurunan kadar oksigen sehingga ini akan mempengaruhi kelangsungan hidup suatu organisme yang hidup dalam lingkup perairan (Susanto, 1991).
Hubungan grafik TSS dan densitas plankton adalah berbanding lurus, yaitu jika TSS tinggi, maka densitas plankton juga tinggi. Namun jika TSS dan densitas plankton itu tinggi, maka kecerahan akan rendah. Hal ini dikarenakan TSS dan plankton akan menghalangi sinar matahari untuk masuk ke dalam air.
Dari grafik DO, dapat diketahui nilai DO tertinggi berada pada stasiun tiga sedangkan nilai DO terendah berada pada stasiun dua. DO yang ada dihasilkan oleh fitoplankton yang melakukan fotosintesis. Sehingga dapat diketahui bahwa jumlah fitoplankton terbanyak berada pada stasiun tiga sedangkan jumlah fitoplankton paling sedikit berada pada stasiun dua. Sumber utama oksigen dalam suatu perairan berasal dari suatu proses difusi dari udara bebas dan hasil fotosintesis organisme yang hidup dalam perairan tersebut (Salmin, 2000).
Dari grafik BOD dapat diketahui bahwa kadar BOD tertinggi berada pada stasiun tiga sedangkan kadar BOD terendah berada pada stasiun empat. Semakin banyak bahan organik dalam air, maka semakin besar BOD yang diperoleh, sedangkan DO akan makin rendah (Agusnar, 2008). Jadi seharusnya grafik BOD berbanding terbalik dengan DO. Namun tidak demikian¸ karena BOD bukan hanya berkaitan dengan DO, tetapi juga berakaitan dengan bahan organik.
Dari grafik bahan organik dapat diketahui bahwa stasiun dua memiliki kandungan bahan organik tertinggi sedangkan stasiun empat memiliki kandungan bahan organik terendah. Seperti yang sudah disebutkan pada pembahasan TSS, grafik bahan organik seharusnya berkebalikan dengan grafik TSS. Namun terjadi penyimpangan pada stasiun dua yang mempunyai bahan organik tinggi. Hal ini terjadi karena bahan organik bukan hanya dipengaruhi oleh TSS, tetapi juga jumlah organisme yang ada di dalam perairan tersebut. Semakin banyak organisme air yang ada maka semakin banyak jumlah bahan organik yang ada. Semua bahan organik mengandung karbon (C) berkombinasi dengan satu atau lebih elemen lainnya. Bahan organik berasal dari tiga sumber utama yaitu Alam, misalnya minyak nabati dan hewani, lemak hewani, alkaloid, selulosa, kanji, gula dan sebagainya. Sintesis, yang meliputi semua bahan organik yang diproses oleh manusia. Fermentasi, misalnya alkohol, aseton, gliserol, antibiotika, dan asam; yang semuanya diperoleh melalui aktivitas mikroorganisme (Effendi, 2003).
Hubungan dari ketiga grafik tersebut adalah BOD berbanding terbalik dengan DO. Kadar BOD dipengaruhi oleh bahan organik yang diuraikan. BOD adalah jumlah oksigen terlarut yang dibutuhkan oleh organisme untuk mengoksidasi bahan-bahan buangan dalam air. Dengan demikian bahan organik akan rendah jika BOD tinggi karena organisme pengurai memiliki BOD yang cukup untuk menguraikan bahan organik yang ada.
Pada grafik CO2, hanya stasiun dua yang memiliki CO2 bebas. Hal ini juga berkaitan dengan fitoplankton yang ada dalam perairan karena fitoplankton dapat melakukan fotosintesis. Fotosintesis membutuhkan CO2 untuk sumber karbon dan akan menghasilkan O2. CO2 yang bernilai nol menunjukkan keberlimpahan fitoplankton tinggi karena semua CO2 digunakan untuk melakukan fotosintesis dan menghasilkan O2 yang banyak. Sumber utama oksigen dalam suatu perairan berasal dari suatu proses difusi dari udara bebas dan hasil fotosintesis organisme yang hidup dalam perairan tersebut (Salmin, 2000). Sehingga grafik CO2 berbanding terbalik dengan grafik DO.
Pada alkalinitas, tingkat alkalinitas tertinggi ada pada stasiun dua dan yang terendah ada pada stasiun empat. Alkalinitas merupakan kemampuan air untuk mempertahankan pH. Alkalinitas dipengaruhi oleh ion karbonat dan ion bikarbonat yang terlarut dalam air. Sehingga stasiun dua merupakan stasiun yang paling bisa mempertahankan pH sedangkan stasiun empat merupakan stasiun yang tidak terlalu bisa mempertahankan pH dibanding yang lain. Alkalinitas sendiri dapat diartikan sebagai nilai yang menunjukkan seberapa kuat suatu perairan mempertahankan pH.
Dari grafik pH, dapat diketahui pH tertinggi berada pada stasiun tiga sedangkan pH terendah berada pada stasiun dua. Menurut Effendi (2003), pH 7 dikatakan netral, pH di atas, 7 dikatakan basa, dan pH di bawah 7 dikatakn asam. Kisaran pH yang baik yaitu berkisar antara 7 – 8. Sehingga semua pH stasiun masih dapat dikatakan memiliki pH yang baik.
Konsentrasi ion H atau pH sangat dekat dengan CO2. CO2 memasuki reaksi kimia dengan air membentuk H2CO3 pada gilirannya bereaksi dengan batu kapur membentuk CO32- dan HCO3- (Odum, 1971). Alkalinitas sendiri berfungsi sebagai buffer agar perairan tidak terlalu asam atau tidak terlalu basa. Jika kadar CO2 tinggi maka alkalinitas juga tinggi. Hal ini dikarenakan CO2 bisa bereaksi untuk membentuk karbonat dan bikarbonat.
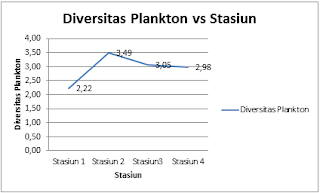
Dari grafik di atas dapat diketahui bahwa diversitas plankton tertinggi berada pada stasiun dua sedangkan diversitas plankton terendah berada pada stasiun satu. Tabel klasifikasi kualitas perairan berdasarkan indeks diversitas Shannon-Wiener dapat dilihat sebagai berikut:
Dari kedua tabel, dapat diketahui bahwa semua stasiun belum tercemar. Untuk kualitas perairannya, stasiun satu sedang, stasiun tiga dan empat baik, dan stasiun empat sangat baik.
Dilihat dari indeks diversitas planktonnya, dapat disimpulkan bahwa stasiun dua memiliki kualitas perairan sungai yang paling baik karena diversitas plankton paling tinggi dan stasiun satu memiliki kualitas perairan sungai paling buruk jika dibandingkan stasiun lain. Menurut tabel kualitas perairan, stasiun dua juga memiliki kualitas perairan sangat baik.
KESIMPULAN
Dari hasil praktikum, dapat disimpulkan bahwa :
1. Ekosistem lentik merupakan ekosistem dengan karakteristik perairan yang menggenang serta memiliki faktor pembatas berupa suhu, DO, CO2 bebas, bahan organik, BOD5, pH, alkalinitas, TSS, dan kecerahan.
2. Pengambilan data pada praktikum ini menggunakan alat ukur secara langsung. Ada juga yang menggunakan metode Gravimetri, metode Alkalimetri, metode Shannon-Wiener dan metode Winkler.
3. Parameter yang ada sangat berpengaruh terhadap komunitas biota perairan. Contohnya semakin tinggi alkalinitas pH akan semakin mendekati netral.
4. Berdasarkan klasifikasi kualitas perairan dengan acuan indeks diversitas Shannon-Wiener , stasiun terbaik dengan kualitas perairan paling baik adalah stasiun dua.
DAFTAR PUSTAKA
Agusnar H. 2008. Pencemaran Air Limbah. Universitas Sumatera Utara. Medan
Barus, T.A. 2004. Pengantar Limnologi. Universitas Sumatera Utara. Medan.
Cole, G.A. 1998. Textbook of Limnologi. 3rd Edition. Wave Land Press Inc. Illions. USA.
Effendi, H. 2003. Telaah Kualitas Air bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Kanisius. Yogyakarta.
Khairuman. 2003. Pembenihan dan Pembesaran Gurami Secara Intensif. Agromedia Pustaka. Jakarta.
Lee, T. D. 1978. Handbook of Variables of environmental Impact Assesment. An Arbor Science Publisher Inc. Arbor.
Odum, E.P. 1971. Fundamentals of Ecology. 3rd edition. W.B. Saunders Company. Philadelphia.
Paney, A.L. 1986. The Ecology of Tropical Lake and Rivers. John Willey and Sons. New York.
Pratiwi, et al. 2004. Panduan Pengukuran Kualitas Air Sungai. Institut Pertanian Bogor. Bogor.
Probosunu, N., 2004. Ekotoksikologi dan Pengendalian Pencemaran Perairan. Bahan Ajar. Jurusan Perikan Fakultas Pertanian Universitas Gadjah Mada.
Rumihat, Mamat. 2007. Ilmu Pengantar Sosial. Grafindo Media Pratama. Jakarta.
Salmin, 2000. Kadar Oksigen Terlarut di Perairan Sungai Dadap. Goba. Muara.
Susanto, 1991. Membuat Kolam Ikan. Penebar Swadaya. Jakarta.
Soegianto,A. 1994. Ekologi Kuantitatif Metode Analisis Populasi Komunitas. Usaha Nasional. Jakarta.
Tarigan, M.S. dan Edward. 2003. Kandungan Total Zat Padat Tersuspensi (Total Suspended Solid) Di Perairan Raha, Sulawesi Tenggara. MAKARA, SAINS, VOL. 7, NO. 3. LIPI.
Wibisono. 2005. Hikmah Kelimpahan Plankton. Universitas Sumatera Utara. Medan.
Demikianlah Info postingan berita LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN
terbaru yang sangat heboh ini LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN, mudah-mudahan bisa memberi manfaat untuk anda semua. baiklah, sekian info artikel kali ini.
Anda sedang membaca posting tentang LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN dan berita ini url permalinknya adalah https://nyimakpelajaran.blogspot.com/2016/11/laporan-ekosistem-danau-ekologi-perairan.html Semoga info lowongan ini bisa bermanfaat.









0 Response to "LAPORAN EKOSISTEM DANAU EKOLOGI PERAIRAN"
Posting Komentar